Ковалентная связь. Разбираем задачи, закрепляем тему
История
С момента открытия атомов и молекул исследователи долгое время задумывались над вопросом, какие силы объединяют микрочастицы в молекуле.
В 1897 году Джозеф Джон Томсон выдвинул теорию, что атомы удерживаются рядом благодаря переносу электронов от одного атома к другому и образованию электронных связей. И был прав. Вклад Томсона в науку был отмечен Нобелевской премией в 1906 году за «изучение прохождения электрического тока через газы».
Исследования продолжились, и в 1916 году американский физико-химик Гильберт Ньютон Льюис объяснил это явление, предложив теорию электронной химической связи. В своих опытах ученый заметил, что наиболее устойчивы при взаимодействии электронные оболочки атомов благородных газов. А атомы других веществ стремятся сделать свою энергетическую оболочку похожей на оболочку благородного газа, расположенного в том же периоде. И для этого присоединяют или отдают электроны. Познакомиться с биографией ученого можно в учебнике Химия 8 класс под редакцией В.В. Еремина на странице 218.
Исследователь предложил графическую модель структуры молекулы, в которой электроны обозначены точками, а связи черточками.
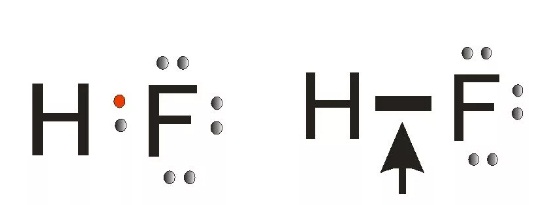
Правило октета
Льюис сформулировал принцип «октета». Согласно этому правилу, при создании молекулы атомы стараются достигнуть восьмиэлектронной валентной оболочки, попарно объединяя электроны, находящиеся на внешней орбитали. По важности это открытие сопоставимо с открытием периодического закона Д.И. Менделеевым.
Заглянем в Периодическую таблицу. В первом периоде находятся водород и гелий. Общее у этих двух газов — одна орбиталь. А вот количество электронов различно: у водорода один, у гелия два. Как мы помним, на первой орбитали у любого элемента могут поместиться всего лишь два электрона. И поскольку орбиталь гелия максимально заполнена — это инертный газ, который не вступает в химические реакции. А вот водород ищет себе пару и объединяется в двухатомные молекулы H2 или образует соединения с другими элементами. В остальных периодах на внешней орбитали могут разместиться восемь электронов.

Механизмы образования связи
Взаимодействие, возникающее при образовании общих электронных пар, называется ковалентная химическая связь. При образовании химической связи выделяется энергия в количестве, необходимом для разъединения атомов на расстояние, при котором взаимодействие стало бы невозможным. Такой тип связи характерен для большинства соединений.
Взаимодействие между атомами различных веществ может происходить двумя способами.
- В первом варианте два атома, у которых на внешнем энергетическом уровне находится по одному свободному электрону, образуют общую пару. Такой механизм взаимодействия называют обменным.
- В некоторых случаях у одного атома есть пара электронов, а у другого свободная орбиталь, которую он предоставляет для взаимодействия. Такой механизм называют донорно-акцепторным.
От электроотрицательности атомов и их способности притягивать электроны зависит, какая ковалентная связь образуется в молекуле.
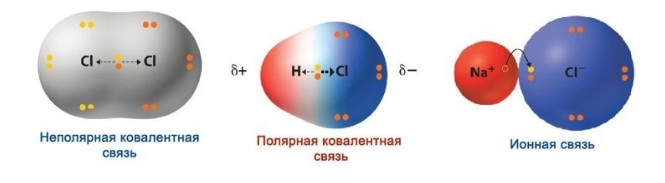
В месте перекрывания электронных облаков создается зона повышенной электронной плотности. Если электроотрицательность элементов равна, электронное облако находится на одинаковом расстоянии от центров атомов, входящих в электронную пару, и образуется ковалентная неполярная связь.
Если электроотрицательность различна, происходит сдвиг электронного облака в сторону центра с большей электроотрицательностью, то есть образуются молекула с двумя полюсами (диполь). Самый простой пример диполя — молекула воды. Данный тип связи и есть ковалентная полярная связь.
Ионная связь — вариант крайне полярной ковалентной связи.
Помимо полярности, ковалентная связь соединения характеризуется и другими параметрами:
- Длиной связи — чем меньше длина, тем прочнее связь.
- Энергией связи — чем больше выделяется энергии при образовании молекулы, тем стабильнее молекула.
- Кратностью связи — число общих электронных пар между атомами. Кратность связи такова, что обеспечивает заполнение внешней электронной оболочки до 8 электронов у обоих атомов. Чем больше кратность связи, тем прочнее ковалентная связь молекулы.
Примеры и задачи
Чтобы закрепить тему, разберем задачу из учебника Химия 8 класс под редакцией В.В. Еремина.
Даны три электронные формулы:
![]() .
.
Какие из перечисленных ниже формул веществ соответствуют каждой из них: NH3, HCl, O2, F2, N2, H2, HBr, Cl2?
Начнем с задания под буквой а.
Поскольку буквенные обозначения элементов разные, следовательно, и вещества в состав молекулы входят разные. Значит, можем вычеркнуть O2, F2, N2, H2 и Cl2.
В состав молекулы входят два атома различных веществ, соответственно, NH3, в молекулу которого входит 4 атома, также вычеркиваем.
У нас остаются HCl и HBr.
И Cl и Br являются элементами VII группы Периодической таблицы, и на внешнем энергетическом слое у них 7 электронов. Значит, оба вещества подходят.
С остальными двумя примерами попробуйте справиться сами.
#ADVERTISING_INSERT#