Комментарии к решениям заданий ЕГЭ по химии
Задание №1
Осадок, полученный при взаимодействии растворов хлорида железа (III) и нитрата серебра, отфильтровали. Фильтрат обработали раствором едкого кали. Выпавший осадок бурого цвета отделили и прокалили. Полученное вещество при нагревании реагирует с алюминием с выделением тепла и света. Составьте уравнения четырех описанных реакций.
Решение:
при взаимодействии как солей соляной кислоты, так и самой кислоты с нитратом серебра образуется АgCl – нерастворимое в воде и кислотах творожистое вещество белого цвета (уравнение 1); эта реакция является качественной на хлорид-ион.
1) 3AgNO3 + FeCl3 = 3AgCl(осадок) + Fe(NO3)3
Фильтрат-раствор, прошедший через фильтр, который задерживает нерастворимые вещества. Взаимодействие растворимых солей с растворами щелочей-способ получения нерастворимых оснований (уравнение 2)
2) Fe(NO3)3 + 3KOH = 3KNO3 + Fe(OH)3(осадок)
Fe(OH)3 – нерастворимое вещество бурого цвета, амфотерный гидроксид, разлагается при нагревании на оксид металла и воду (уравнение 3).
3) Fe(OH)3 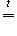 Fe2O3 + 3H2O
Fe2O3 + 3H2O
Восстановление металлов из их оксидов с помощью алюминияпромышленный способ получения многих металлов (алюмотермия); реакция экзотермическая, сопровождается выделением тепла, света и плавлением реакционной массы (уравнение 4)
4) Fe2O3 + 2Al = Al2O3 + 2Fe
Задание №2
Продукты разложения хлорида аммония последовательно пропустили через нагретую трубку, содержащую оксид меди(II), а затем через склянку с оксидом фосфора(V). Составьте уравнения четырёх описанных реакций.
Решение:
Соли аммония и кислот, для которых нехарактерны окислительные свойства (NH4Cl, (NH4)2CO3), при нагревании разлагаются на аммиак NH3 и кислоту (уравнение 1)
1) NH4Cl 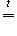 NH3(газ) + HCl(г)
NH3(газ) + HCl(г)
Оксид меди (II) – основный оксид, кислоты реагируют с основными оксидами с образованием солей (уравнение2)
2) 2HCl + СuO = CuCl2 + H2O
Аммиак, в котором азот находится в низшей степени окисления N–3, проявляет восстановительные свойства и восстанавливает среднеактивные и малоактивные металлы из их оксидов (уравнение 3)
3) 2NH3(г) + 3СuO = 3Cu(осадок) + N2(газ) + 3H2O
При взаимодействии P2O5 с водой, в зависимости от соотношения реагентов и температуры, могут образовываться фосфорные кислоты (H4P2O7, HPO3, H3PO4) (уравнение 4); азот с P2O5 не реагирует
4) P2O5 + 3H2O = 2H3PO4
Задание №3
Газ, выделившийся при взаимодействии хлороводородной кислоты с перманганатом калия, реагирует с железом. Продукт реакции растворили в воде и добавили к нему сульфид натрия. Более легкое из образовавшихся нерастворимых веществ отделили и ввели в реакцию с горячей концентрированной азотной кислотой.
Составьте уравнения четырёх описанных реакций.
Решение:
Взаимодействие соляной кислоты с перманганатом калия является способом получения хлора (уравнение 1)
1) 16HCl + 2KMnO4 = 2KCl + 2MnCl2 + 5Cl2(газ) + 8H2O
Железо взаимодействует с сильными окислителями с образованием соединений железа в степени окисления +3 (уравнение 2)
2) 2Fe + 3Cl2(г) = 2FeCl3
Железо в степени окисления +3 проявляет свойства окислителя, поэтому может взаимодействовать с восстановителем (сульфид натрия восстановитель, так как содержит серу в степени окисления S–2), образуя соединения двухвалентного железа (уравнение 3)
3) 2FeCl3 + 3Na2S = S(осадок) + FeS(осадок) + 6NaCl
Горячая азотная кислота окисляет серу до высшей степени окисления +6 (до H2SO4), азот при этом восстанавливается до N+4(до NO2) (уравнение 4)
4) S + 6HNO3(конц., горяч) = H2SO4 + 6NO2(газ) + 2H2
Задание №4
При сжигании на воздухе простого вещества жёлтого цвета образуется газ с резким запахом. Этот газ выделяется также при обжиге некоторого минерала, содержащего железо, на воздухе. При действии разбавленной серной кислоты на вещество, состоящее из этих же элементов, что и минерал, но в другом соотношении, выделяется газ с запахом тухлых яиц. При взаимодействии выделившихся газов друг с другом образуется исходное простое вещество. Составьте уравнения четырёх описанных реакций.
Решение.
Простое вещество желтого цвета, горящее на воздухе с выделением газа с резким запахом, – сера (уравнение 1)
1) S + O2 = SO2(г)
Вещества, содержащие железо и серу: минерал пирит FeS2 и сульфид железа (II) (уравнения 2 и 3)
2) 4FeS2 + 11O2 = 2Fe2O3 + SO2(г)
3) FeS + H2SO4 = FeSO4 + H2S(г)
При взаимодействии оксида серы (IV) и сероводорода первый проявляет свойства окислителя, второй-восстановителя) и образуется простое вещество-сера (уравнение4)
4) SO2 + 2H2S = 3S(осадок) + 2H2O
Задание №5
После кратковременного нагревания неизвестного порошкообразного вещества оранжевого цвета начинается самопроизвольная реакция, которая сопровождается изменением цвета на зелёный, выделением газа и искр. Твердый остаток смешали с едким калии нагрели, полученное вещество внесли в разбавленный раствор соляной кислоты, при этом образовался осадок зелёного цвета, который растворяется в избытке кислоты. Составьте уравнения четырёх описанных реакций.
Решение:
Вещество оранжевого цвета, которое разлагается с изменением цвета на зелёный, – бихромат аммония (NH4)2Cr2O7 (уравнение 1)
1) (NH4)2Cr2O7 = N2(г) + Cr2O3 + 4H2O
Cr2O3 – вещество зелёного цвета, – амфотерный оксид и будет реагировать с безводной щелочью с образованием соли (уравнение 2)
2) Cr2O3 + 2KOH = 2KCrO2 + H2O
В воде, в присутствии небольшого количества кислоты, KCrO2 будет гидролизоваться с образованием нерастворимого амфотерного гидроксида хрома(III) (уравнеие 3)
3) KCrO2 + H2O + HCl = KCl + Cr(OH)3(осадок)
Амфотерный гидроксид хрома (III) растворяется в избытке кислоты с образованием Cr+3, имеющий зелёный цвет (уравнение 4).
4) Cr(OH)3(осадок) + 3HCl(изб) = СrCl3 + 3H2O





















Оставьте свой комментарий к работе, нажав на кнопку «Написать». Расскажите, что именно вас не устраивает в работе, а если вы считаете, что работа содержит ошибки и неточности – нажмите на соответствующую галочку в форме отклика.
Внимание! Администрация сайта rosuchebnik.ru не несет ответственность за содержание методических разработок, а также за соответствие разработки ФГОС.